Inscription / Connexion Nouveau Sujet
acide ascorbique : titrage
bonsoir,
j'ai un peu de mal pour quelque question:
L'acide ascorbique, de formule brute C6H8O6 est communément appelé Vitamine C. Il est vendu sous forme de comprimés.
Le but de cette étude est de déterminer, par dosage, la masse d'acide ascorbique présente dans un comprimé. Pour cela, on dissout un comprimé de Vitamine C du commerce dans 100 mL d'eau distillée et l'on dose 100 mL de solution par une solution d'hydroxyde de sodium de concentration 0,32 mol .L-1
Le graphique donnant les variations de la conductance G de la solution en fonction du volume v de solution d'hydroxyde de sodium versé est donné ci-contre.
a. Comment procéder pour réaliser le dosage conductimétrique de la solution d'acide ascorbique par la solution d'hydroxyde de sodium ? Faire un schéma.
b. Ecrire l'équation de la réaction entre les solutions d'acide ascorbique et d'hydroxyde de sodium. Préciser la formule de la base conjuguée de l'acide ascorbique.
c. Interpréter qualitativement l'évolution de la conductivité (On précisera en particulier les espèces ioniques présentes avant et après l'équivalence).
d. Dresser le tableau permettant de suivre l'évolution de la réaction au cours du dosage.
e. Le volume à l'équivalence se trouvant à l'intersection des deux portions de droite du graphique G(4v). Déterminer la valeur du volume à l'équivalence et la concentration de la solution de Vitamine C réalisée.
f. En déduire la masse d'acide ascorbique contenue dans un comprimé. Ce résultat est-il compatible avec l'indication 500 du fabricant « Vitamine C 500»?
quelqu'un peut-il m'aider pour la question a et c?
merci de votre aide

Salut !
!
a) Je pense que tu as fait le schéma du montage conductimétrique?
b) Commence par trouver les couples et la base conjuguée de l'acide ascorbique.
c) Appuies-toi en particulier sur la conductivité molaire ionique de l'ion hydroxyde et sur ton équation
d) Je te laisse faire, la réaction est équimolaire donc pas besoin de faire attention aux coeff
e) Détermine Véq graphiquement. Je ne peux pas agrandir ton image mais je pense qu'elle se situe (ou qu'elle est même) de 9,00 mL.
Pour la concentration sers-toi de la déf de la conductance (car ton graphe te donne la conductance). Mais de toute façon tu peux faire facilement le lien avec la conductivité.
f) m = nM. En principe tu dois trouver 500 mg.
Bon je ne t'ai pas aidé que pour a) et c), c'est à titre d'indice ou de vérification
Voici un exemple en attendant de trouver mieux: 
Je te l'aurais bien dessiné mais je viens de récupérer mon ordi et je n'ai pas encore installé l'imprimante
Deux autres possibilités selon le matos utilisé:
-avec un conductimètre (ne tient pas compte des noms des solutions titrante et titrée): 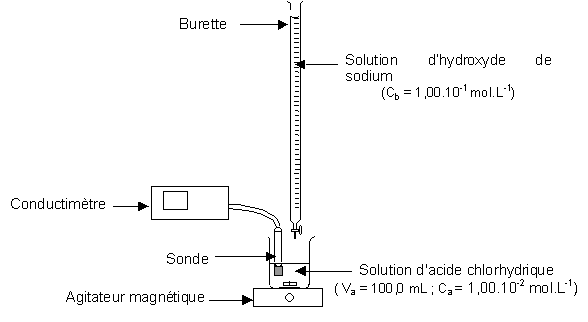
-avec mesure de la conductance (voltmètre/ampéremètre/cellule conductimétrique): 
merci!
pouvez m'aidez en indiquant les quantités de volumes que l'on doit prélever, et le reste des manipulations?
merci de votre aide


